新版GMP环境下,厚永赋能医疗器械公司的新机遇
先花1分钟,看厚永如何用实力对标新版GMP
2026年11月1日,新版《医疗器械生产质量管理规范》(GMP)将正式实施。新规从13章增至15章,新增“质量保证”“验证与确认”“委托生产”三大核心章节,对人员、硬件、体系提出更高要求。成本上升、合规风险增加,企业该如何应对?
作为深耕行业的一站式CDMO平台,东莞厚永医疗为您解读新旧GMP的核心差异,并告诉您:在变革的浪潮中,如何借助专业平台的力量,将“挑战”转化为“机遇”。
新旧 GMP 核心差异对比:门槛高在哪?
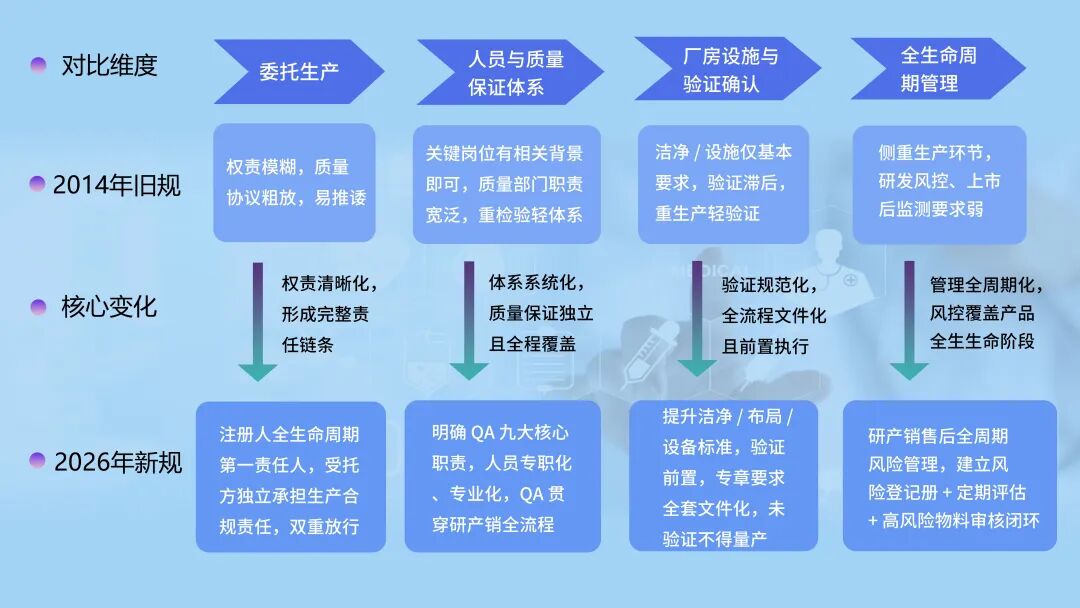
小结:新规的变化,意味着医疗器械企业不能再依靠“低成本凑合”的方式生存。人员要更精、硬件要更硬、体系要更严、数据要更全、责任要更清、管理要更前——而这些,恰恰是企业成本上升的源头,也是专业化CDMO平台价值凸显的关键所在。
新规下企业四大成本飙升及厚永专属解决方案

痛点
Pain point -
需组建专职 QA 团队,而高端质量人才年薪高,普遍在20-40万区间,人力成本大幅翻倍。
厚永方案

痛点
Pain point -
车间升级改造耗资数百万,验证费用高、周期长,严重拖慢产品上市。
厚永方案

痛点
Pain point -
数字化合规体系搭建投入大、难度高,中小企业负担重。
厚永方案

痛点
Pain point -
全周期投入大,委托生产权责不清,易引发飞检与注册风险。
厚永方案
结语
新版GMP的实施,是一场医疗器械行业的“供给侧改革”,门槛提升的背后,更是行业规范化发展的新机遇。厚永医疗以专业 CDMO 能力,全面对标 2026 版 GMP,为企业提供从研发到上市的全流程合规支持,让企业告别高成本、高风险的独自摸索,轻装上阵抓住新规下的行业新机遇!

联系我们
手机丨13590196539(赵)
电话丨0769—22229890
本篇文章来源于微信公众号:厚永医疗科技






